以顺铂为代表的铂类药物是实体瘤临床治疗的一线用药,凭借其明确的DNA抗肿瘤机制被广泛应用于多种恶性肿瘤的治疗。然而,药物低选择性带来的严重毒副作用始终是限制其临床应用的核心瓶颈。为解决这一难题,围绕化学稳定性更高、可修饰性更强的Pt(IV)核心开发前药体系正成为铂类抗肿瘤药物的研究热点。多肽作为靶向载体,兼具优异的组织穿透能力、抗体级高特异性与低成本化学合成的优势,成为铂药靶向递送的重要研究方向。基于此,山东第一医科大学药学院(药物研究所)牟艳玲/张春雨课题组充分利用多肽可设计、易修饰、靶向性强的特点,成功制备了细胞核靶向Pt (IV)-TAT前药,该药物在细胞水平及小鼠活体水平均表现出优异的抗肿瘤功效,且具有较低的系统毒性。机制研究证实,Pt(IV)-TAT可以被肿瘤细胞高效摄取,能更高效的进入细胞核并与细胞核内DNA结合,通过诱导DNA损伤激活Caspase-3/PARP凋亡通路,最终引发肿瘤细胞凋亡。相关成果近期以研究论文的形式发表在ACS Applied Materials & Interfaces期刊(图1)。
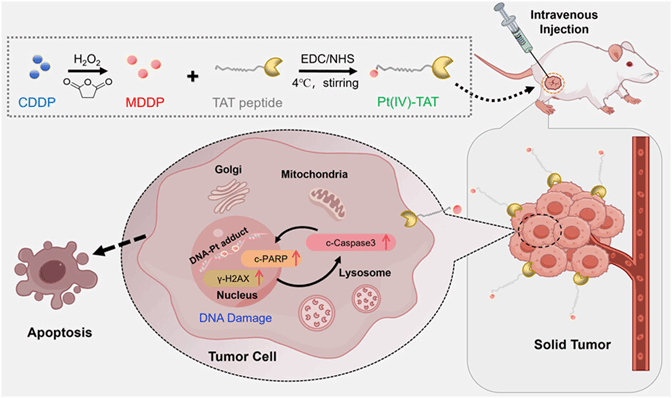
图1. Pt (IV)-TAT药物制备过程及低毒靶向抗肿瘤机制示意图
课题组还围绕靶向多肽修饰密度与铂药活性的构效关系开展了更深入的研究。Pt(IV)前药的轴向配体修饰是实现靶向递送、药效优化的核心策略。然而靶向配体的修饰密度与药物细胞摄取、还原活化、抗肿瘤活性之间的内在关联尚不明确。因此,课题组通过分子设计与反应条件调控,分别合成了单分子TAT多肽修饰的s-CisPt (IV)-TAT与双分子TAT多肽修饰的d-CisPt (IV)-TAT两种Pt (IV)前药,并系统对比了两者的理化性质、细胞毒性、摄取效率与抗肿瘤作用机制。研究结果表明,双分子多肽修饰的Pt(IV)药物产生更高的空间位阻,降低了肿瘤细胞对药物的摄取效率,最终导致细胞核内铂含量、DNA结合效率与DNA损伤能力显著低于单取代药物。该研究首次系统揭示了核靶向多肽修饰的Pt(IV)药物的结构-活性关系,为多肽偶联化疗药物的理性设计中功能密度与生物学性能的平衡提供了重要的理论参考与实验依据。相关成果近期以研究论文的形式发表在Molecular Pharmaceutics期刊(图2)。
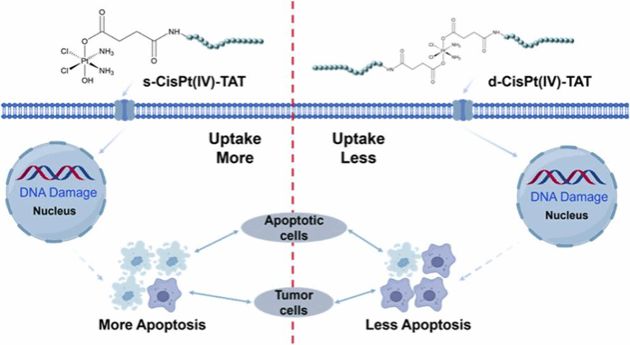
图2. 单/双分子取代Pt (IV)药物的细胞摄取、DNA损伤与凋亡诱导差异示意图
文章原文链接:
(1) Ruihan Li, Chuanke Chong, Mei Liu, Xuan Yin, Yan Li, Ying Li, Qingqiang Yao, Yanling Mu,* Chunyu Zhang,* Platinum(IV) Prodrug-Coupled TAT Nuclear-Targeting Peptide for Drug Delivery and High Antitumor Efficacy with Low Toxicity. ACS Applied Materials & Interfaces 2025, 17, 41792-41805. https://doi.org/10.1021/acsami.5c09286
(2) Ruihan Li, Xuan Yin, Chuanke Chong, Yan Li, Qingqiang Yao, Yanling Mu,* Chunyu Zhang,* Exploring the Relationships between Targeted Structures and Antitumor Activities of Nuclear-Targeted Polypeptide-Functionalized Platinum(IV) Prodrugs. Molecular Pharmaceutics 2025, 22, 6349-6356. https://doi.org/10.1021/acs.molpharmaceut.5c01110